La stimulation magnétique transcrânienne (TMS) est une procédure de stimulation non invasive permettant d’agir de façon focalisée sur une région cérébrale particulière au moyen de champs électromagnétiques transitoires. Elle peut être utilisée comme thérapie dans la dépression, la maladie de Parkinson ou encore dans les troubles obsessionnels compulsifs chez des patients résistants aux traitements médicamenteux. A l’Institut du cerveau, des chercheurs ont également montré des effets durables de la TMS dans la rééducation après un accident vasculaire cérébral.
Les effets thérapeutiques de la TMS chez l’homme
On considère généralement que les stimulations magnétiques de haute intensité utilisées chez l’homme sont capables de générer un champ électrique suffisant pour moduler l’activité des neurones : déclencher des influx nerveux codant l’information cérébrale et induire des phénomènes de plasticité dans les réseaux neuronaux de la région ciblée.
Mais bien que son efficacité thérapeutique soit reconnue dans un certain nombre de cas, les mécanismes qui permettent à la TMS de rétablir ou modifier durablement les activités neuronales dans les régions cérébrales stimulées restaient encore mal connus.
La TMS à l’échelle des neurones
Pour la première fois, Manon Boyer et Séverine Mahon, respectivement doctorante et chercheuse dans l’équipe « Excitabilité cellulaire et dynamiques des réseaux neuronaux » en collaboration avec le Dr Antoni Valero-cabre Equipe « FRONTLAB: Fonctions et dysfonctions de systèmes frontaux (institutducerveau-icm.org) à l’Institut du cerveau, ont montré directement l’effet de la TMS de basse intensité sur l’excitabilité et l’activité spontanée des neurones du cortex cérébral, activité qui permet à ces cellules de communiquer entre elles et de transmettre l’information aux organes périphériques et aux muscles. Ces travaux sont publiés dans The Journal of Physiology.
Les chercheuses ont combiné l’application de stimulations magnétiques répétées de basse intensité sur le cortex somato-sensoriel d’un modèle expérimental avec un enregistrement intracellulaire de l’activité électrique des neurones sous-jacents ; technique permettant de comprendre l’effet de la TMS vu de l’intérieur des neurones.
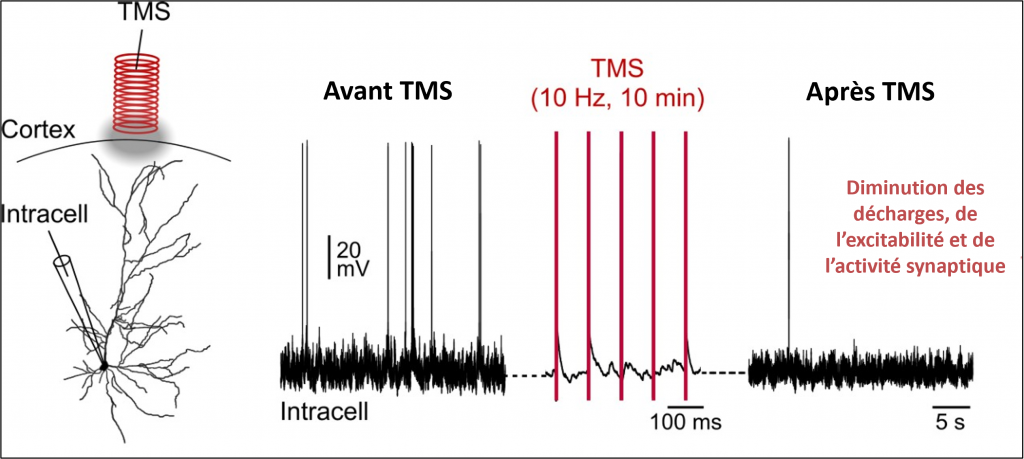
Enregistrement de l’activité électrique intraneuronale avant et après TMS
Elles ont ainsi montré que la TMS répétitive de basse intensité peut également déclencher des potentiels d’action dans les neurones et induire une plasticité qui s’exprime par une diminution durable de l’activité spontanée des neurones, de leur excitabilité et de l’amplitude des événements synaptiques (reflétant une diminution de la transmission des informations entre les neurones). Ces changements ne sont pas reproduits en stimulant directement les cellules avec un courant électrique de même intensité, démontrant directement le rôle spécifique du champ magnétique.
Les nouvelles pistes thérapeutiques de la TMS
En conclusion, ces travaux montrent que la TMS de faible intensité a des effets durables sur l’excitabilité et l’activité de décharge des neurones du cortex et ouvrent de nouvelles pistes thérapeutiques pour les pathologies dans lesquelles on observe une hyperexcitabilité cérébrale comme l’épilepsie ou le syndrome de Gilles de la Tourette.
En effet dans l’épilepsie on observe une activité électrique anormalement haute d’un ensemble de neurones du cortex cérébral qui forment alors un foyer épileptique.
Ces travaux montrent que la TMS de basse intensité, thérapeutique non invasive et facilement déployable au chevet du patient constitue une piste très prometteuse pour les patients atteints d’épilepsie










